Mensen met reumatoïde artritis (RA) krijgen meestal van hun reumatoloog te horen dat voeding slechts een beperkte rol speelt bij hun aandoening. Ze bedoelen hiermee te zeggen dat er onvoldoende wetenschappelijk bewijs beschikbaar is dat (gedeeltelijke) vervanging van medicatie door voedingsinterventies rechtvaardigt.1 Toch wil dat niet zeggen dat voeding geen of slechts een beperkte rol speelt bij het ontstaan en de progressie van deze ziekte. Bijna 25% van de RA-patiënten meldt een effect van voeding op hun ziekteactiviteit.2 Onderstaand een overzicht van de kennis over voeding en suppletie in relatie tot RA tot nu toe.
Het Louis Bolk Instituut deed in 2017 onderzoek naar de invloed van het eetpatroon van mensen met multiple sclerose (n=180) en reuma (n=120) op de klachten die zij ervaren. Het blijkt dat mensen die minder bewerkt voedsel, suikers en koolhydraten binnenkrijgen minder last hebben van hun aandoening bij het dagelijks functioneren.3 Het ging hier om een pilotonderzoek met een observationele onderzoeksopzet. Het belangrijkste doel van het programma was om de haalbaarheid en waardering van een dergelijk leefstijlprogramma te onderzoeken bij deze reumapatiënten. Het genereren van degelijke wetenschappelijke onderbouwing voor het nut van suppletie- en voedingsadviezen bij RA is namelijk complex, omdat onderzoekers problemen ondervinden met rekrutering, therapietrouw en uitval. Het is immers moeilijk om leefstijlverandering op lange termijn vol te houden. Er is continu begeleiding van de deelnemers nodig en tevens zijn er voldoende proefpersonen nodig om te kunnen corrigeren voor variabelen die de ziekteactiviteit kunnen beïnvloeden.
Wat is reumatoïde artritis?
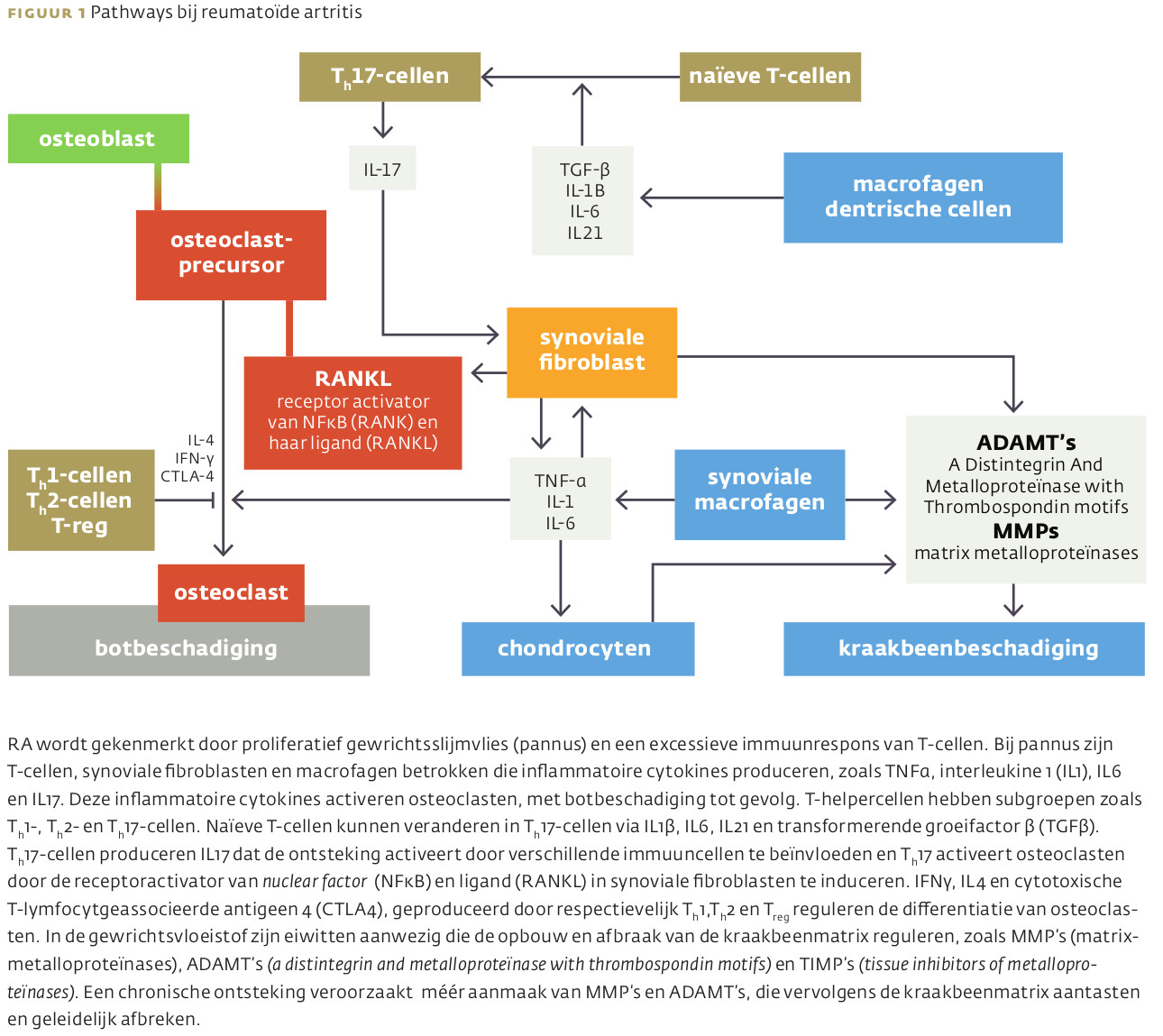
RA is een systemische, slopende en chronisch inflammatoire auto-immuunziekte, waaraan ongeveer 1% van de wereldpopulatie lijdt.4 In Nederland hebben ongeveer 260.000 mensen reumatoïde artritis. Diverse studies houden een mix van omgevingsfactoren en genetische factoren verantwoordelijk voor het ontstaan van de ziekte. Genetische factoren zouden voor zeker de helft bijdragen aan het ontstaan ervan.5 De precieze oorzaak van de ziekte, ook wel chronische gewrichtsreuma genoemd, is onduidelijk. In figuur 1 is de huidige kennis omtrent de pathologie van RA schematisch weergegeven.6
Conventionele behandeling
 Bij de conventionele behandeling van reuma staan medicijnen centraal met als doel het ziekteproces af te remmen en tot rust te brengen. Het gaat om algemene pijnstillers (paracetamol), NSAID’s, corticosteroïden, klassieke reumamedicijnen (afweeronderdrukkers), biologische medicijnen (werkzame stof is gemaakt door een levend organisme of afkomstig is van een levend organisme) en JAK-remmers (januskinase) die de aanmaak van cytokines verminderen.
Bij de conventionele behandeling van reuma staan medicijnen centraal met als doel het ziekteproces af te remmen en tot rust te brengen. Het gaat om algemene pijnstillers (paracetamol), NSAID’s, corticosteroïden, klassieke reumamedicijnen (afweeronderdrukkers), biologische medicijnen (werkzame stof is gemaakt door een levend organisme of afkomstig is van een levend organisme) en JAK-remmers (januskinase) die de aanmaak van cytokines verminderen.
Darmmicrobioom centraal
Op het moment dat het over voedingsinterventies gaat, ontkomen we niet aan het darmmicrobioom. Er is toenemend bewijs dat een veranderde samenstelling van het darmmicrobioom bij RA-patiënten verantwoordelijk is voor de pathogenese en ziekteprogressie. De link tussen het darmmicrobioom en het immuunsysteem is immers een wetenschappelijk feit.8-13 Het achterliggende mechanisme kenmerkt zich door verhoogde doorlaatbaarheid van epitheelcellen en darmmucosa en verlaagde immuuntolerantie voor de residente microbiota. Beïnvloeding van het darmmicrobioom kan dus een onderdeel zijn van de behandeling van RA.14 Voeding is een van de manieren, naast probiotica en antibiotica, om het microbioom te beïnvloeden en daarmee wellicht ook de ziekteactiviteit.
RA wordt tevens gekenmerkt door de aanwezigheid van antistoffen die lichaamseigen eiwitten herkennen (auto-antistoffen). De meest specifieke en gevoelige auto-antistoffen die in RA-patiënten gevonden zijn, herkennen gecitrullineerde eiwitten.42 Deze auto-antistoffen kunnen al gedetecteerd worden in patiënten met gewrichtsklachten jaren voordat er een definitieve RA-diagnose wordt vastgesteld. De aanwezigheid van de auto-antistoffen tegen gecitrullineerde eiwitten verhoogt in patiënten met gewrichtsklachten de kans op de ontwikkeling van RA aanzienlijk, terwijl bij gediagnosticeerde RA-patiënten de aanwezigheid van deze auto-antistoffen een meer agressief karakter van de ziekte voorspelt. In diverse studies zijn darm- en mondmicrobioom in verband gebracht met citrullinatie dat bijdraagt aan de ontwikkeling van RA.43
Zo zijn er aanwijzingen dat een bacterie (Aggregatibacter actinomycetemcomitans) die een belangrijke rol speelt in het ontstaan van parodontitis, ook de auto-immuniteit in reumatoïde artritis (RA) triggert.66 Infectie met deze bacterie wakkert de productie van gecitrullineerde eiwitten aan. De klinische studies tot nu toe zijn echter klein en kortdurend.44
Voedingsinterventies
Mediterrane voeding
 Mediterrane voeding is voornamelijk gebaseerd op een overwegend plantaardige voeding met vis en een beperkte vleesconsumptie. Een typisch mediterraan voedingspatroon is rijk aan olijfolie, granen, fruit, bonen, noten en zaden en er is een matige consumptie van rode wijn. Het is rijk aan oliezuur (omega-9), omega-3-vetzuren, vezelrijke koolhydraten en fytonutriënten, zoals flavonoïden. Het gunstige effect van mediterrane voeding bij RA is voornamelijk toe te schrijven aan de ontstekingsremmende effecten van de omega-3-vetzuren en antioxidanten.15 Bestanddelen van olijfolie, zoals oliezuur en oleocanthal, hebben natuurlijke anti-inflammatoire eigenschappen.16
Mediterrane voeding is voornamelijk gebaseerd op een overwegend plantaardige voeding met vis en een beperkte vleesconsumptie. Een typisch mediterraan voedingspatroon is rijk aan olijfolie, granen, fruit, bonen, noten en zaden en er is een matige consumptie van rode wijn. Het is rijk aan oliezuur (omega-9), omega-3-vetzuren, vezelrijke koolhydraten en fytonutriënten, zoals flavonoïden. Het gunstige effect van mediterrane voeding bij RA is voornamelijk toe te schrijven aan de ontstekingsremmende effecten van de omega-3-vetzuren en antioxidanten.15 Bestanddelen van olijfolie, zoals oliezuur en oleocanthal, hebben natuurlijke anti-inflammatoire eigenschappen.16
Toch zijn de resultaten van onderzoek niet eenduidig. In sommige studies is vermindering van pijn en ziekteactiviteit te zien bij het volgen van een mediterraan voedingspatroon.17 -19 In een review van prospectieve studies naar het effect van mediterrane voeding op RA-preventie werden in twee van de vier studies verbeteringen vastgesteld op het gebied van pijn en de Health Assessment Questionaire (HAQ-score ). In één studie werd een verlaging van de ‘28 Joint Count Disease Activitity Score’ (DAS28) gevonden. Echter mediterrane voeding was niet geassocieerd met een lager risico op RA.20 In de TOMORROW-studie bleek een hoge inname van enkelvoudig onverzadigde vetzuren een onafhankelijke voorspeller van remissie in de RA-groep op de grens van het statistisch significante.21
Plantaardige voeding
 Uit een recente review van onderzoeken naar RA blijkt dat een plantaardig voedingspatroon helpt om pijn te bestrijden en in het algemeen de kwaliteit van leven te verhogen.22 De auteurs redeneren dat het niveau van inflammatie hierdoor kan worden teruggedrongen. Verder levert gewichtsverlies een belangrijke bijdrage aan verlichting van symptomen. En afvallen is over het algemeen gemakkelijker met vegetarische of veganistische voeding. Tenslotte bevordert plantaardige voeding – met name door het vezelrijke karakter – een gezond microbioom. De bacteriële diversiteit die bij mensen met RA te wensen overlaat, wordt door dergelijke voeding groter.
Uit een recente review van onderzoeken naar RA blijkt dat een plantaardig voedingspatroon helpt om pijn te bestrijden en in het algemeen de kwaliteit van leven te verhogen.22 De auteurs redeneren dat het niveau van inflammatie hierdoor kan worden teruggedrongen. Verder levert gewichtsverlies een belangrijke bijdrage aan verlichting van symptomen. En afvallen is over het algemeen gemakkelijker met vegetarische of veganistische voeding. Tenslotte bevordert plantaardige voeding – met name door het vezelrijke karakter – een gezond microbioom. De bacteriële diversiteit die bij mensen met RA te wensen overlaat, wordt door dergelijke voeding groter.
Een voedingspatroon rijk aan vet en bewerkt vlees is positief geassocieerd met ontstekingsmarkers zoals CRP, IL6 en homocysteïne, terwijl een voeding rijk aan volkoren granen en fruit omgekeerd geassocieerd is met deze biomarkers.23 Het wachten is nu op de resultaten van de ‘Plants for Joints’-studie. In deze studie volgen mensen met artrose en RA een programma van vier maanden waarin ze plantaardig eten, gezond bewegen en ontspannen. Na afloop van de interventie worden alle patiënten nog één jaar gevolgd, waarbij na een half jaar en een jaar een meting wordt gedaan. Gemeten wordt onder andere het lipidenprofiel van het bloed, de bloedglucose en ontstekingsmarkers. Ook wordt ontlasting verzameld om het microbioom in kaart te brengen. Het onderzoek wordt uitgevoerd onder leiding van Dirkjan van Schaardenburg, hoogleraar aan het Amsterdam UMC en hoofd reumatologie bij Reade Amsterdam. Plants for Joints is het eerste grote Nederlandse wetenschappelijke onderzoek naar de invloed van veganistisch eten, gezond bewegen en ontspannen bij mensen RA en artrose. Aanmelden voor deelname van dit onderzoek is nog steeds mogelijk.
Elementaire voeding
Een elementaire voeding is een complete vloeibare voeding met voedingsstoffen in een gemakkelijk opneembare vorm. Het is samengesteld uit aminozuren, vetten, koolhydraten, vitaminen en mineralen en is meestal hypo-allergeen.
In een pilotstudie kregen 30 patiënten met actieve RA gedurende twee weken een elementaire voeding (n=21) of orale prednisolon (15 mg per dag) (n=9).24 De elementaire voeding bleek even effectief als de prednisolon voor het verbeteren van subjectieve parameters in RA, behalve voor de score voor gezwollen gewrichten. Een verbetering van meer dan 20% in de ochtendstijfheid, pijnscore en de score op de schaal van Ritchie werd vastgesteld bij 72% van de groep die elementaire voeding gebruikte en bij 78% van de mensen die prednisolon namen. Echter deze verbeteringen kwamen niet tot uiting in de laboratoriumuitslagen (ESR, CRP, hemoglobine). Bij het stoppen van de elementaire voeding kwamen de symptomen weer terug. De auteurs concluderen dat voedselallergenen vermoedelijk een rol spelen in de pathogenese en progressie van RA.
Eliminatiedieet
 Het is aangetoond dat de darmmucosa van RA-patiënten die NSAID’s gebruiken een hogere doorlaatbaarheid heeft voor allergenen.25 Er is toenemend bewijs dat RA een gastro-intestinale component heeft en zelfs zijn oorsprong vindt in de darm.24 Het is dan ook niet verwonderlijk dat gewrichtssymptomen vaak gepaard gaan met darmgerelateerde aandoeningen zoals coeliakie, bariatrische ingrepen en IBS.26 Mestcellen die geactiveerd zijn in reactie op antigenen, meestal gemedieerd door IgE, zijn in verhoogde mate aanwezig in synoviale weefsels van RA-patiënten.27 Bovendien zijn de conclusies uit diverse onderzoeken dat voedselallergenen potentiéle triggers zijn voor het immuunsysteem. Ze veroorzaken inflammatie via activatie van onder andere macrofagen. De auteurs Van der Laar en Korst van het Jan van Breemeninstituut concludeerden uit hun studie dat er een subgroep van patiënten is waarbij voedselintolerantie de ziekteactiviteit beïnvloedt.28 Onderdeel van de reguliere behandeling van RA is het remmen van TNFα en IL1 en deze inflammatoire mediatoren zijn ook verhoogd bij inname van allergene voeding. Wellicht kan het elimineren van dergelijke allergenen de behoefte aan bepaalde medicatie verminderen.29 Eliminatiediëten waarbij een of meer voedingsmiddelen die als trigger lijken te fungeren uit de voeding geschrapt worden, laten verbetering zien bij RA-patiënten in klinische studies.30,31 De ‘triggerfoods’ lijken sterk individueel bepaald.
Het is aangetoond dat de darmmucosa van RA-patiënten die NSAID’s gebruiken een hogere doorlaatbaarheid heeft voor allergenen.25 Er is toenemend bewijs dat RA een gastro-intestinale component heeft en zelfs zijn oorsprong vindt in de darm.24 Het is dan ook niet verwonderlijk dat gewrichtssymptomen vaak gepaard gaan met darmgerelateerde aandoeningen zoals coeliakie, bariatrische ingrepen en IBS.26 Mestcellen die geactiveerd zijn in reactie op antigenen, meestal gemedieerd door IgE, zijn in verhoogde mate aanwezig in synoviale weefsels van RA-patiënten.27 Bovendien zijn de conclusies uit diverse onderzoeken dat voedselallergenen potentiéle triggers zijn voor het immuunsysteem. Ze veroorzaken inflammatie via activatie van onder andere macrofagen. De auteurs Van der Laar en Korst van het Jan van Breemeninstituut concludeerden uit hun studie dat er een subgroep van patiënten is waarbij voedselintolerantie de ziekteactiviteit beïnvloedt.28 Onderdeel van de reguliere behandeling van RA is het remmen van TNFα en IL1 en deze inflammatoire mediatoren zijn ook verhoogd bij inname van allergene voeding. Wellicht kan het elimineren van dergelijke allergenen de behoefte aan bepaalde medicatie verminderen.29 Eliminatiediëten waarbij een of meer voedingsmiddelen die als trigger lijken te fungeren uit de voeding geschrapt worden, laten verbetering zien bij RA-patiënten in klinische studies.30,31 De ‘triggerfoods’ lijken sterk individueel bepaald.
Een Scandinavische studie toonde aan dat de aanwezigheid antigliadine-antilichamen (AGA) in het bloed, klinisch relevant is bij een subgroep van oudere mensen en dat het geassocieerd is met RA en depressie, die beide ook gelinkt zijn aan coeliakie.32 Glutenvrije voeding lijkt gunstig bij mensen met RA, hoewel het beschikbare bewijs niet eenduidig is.33,34
Er lijkt onvoldoende onderbouwing voor strikte eliminatie van zuivelproducten.35 Moleculair bioloog Van de Loo (RadboudUMC) was er ooit van overtuigd dat het drinken van koemelk te maken heeft met het ontstaan en instandhouding van reuma. Zijn hypothese was dat met het drinken van melk kleine celdeeltjes, extracellulaire blaasjes (EV’s) of exosomen van de koe zelf meekomen. Hij participeerde in onderzoek, waarbij gekeken is of deze EV’s het afweersysteem ontregelen. Het tegendeel bleek waar. Dat is eigenlijk niet verrassend want in de context van inflammatie kunnen EV’s zowel pro‐ als anti-inflammatoire effecten hebben.36 Het onderzoek liet zien dat deze deeltjes, de zogenaamde bovine milk derived extracellular vesicles (BMEVs), een gunstig effect hadden op spontane polyartritis bij muizen met een in IL1Ra‐tekort en geïnduceerde artritis. Orale toediening vertraagt het begin van de ziekte in twee modellen van reumatoïde artritis, vermindert kraakbeenpathologie en beenmerginflammatie, vermindert de cytokinerepons op LPS en er is bewijs voor verminderde Th1- en Th17-spiegels in muizen.37 Er zijn echter nog veel open vragen, namelijk: “Werkt complete melk anders dan alleen hun EV’s? Is rauwe melk anders dan bewerkte melk? Hoe heterogeen zijn EV’s? Wat is het werkingsmechanisme, kunnen ook andere ziekten baat hebben bij EV’s uit koemelk?”
Periodiek vasten
Onderzoek bij mensen laat zien dat minder calorieën eten het risico op ouderdomsziekten doet afnemen, en het aantal gezonde levensjaren verhoogt.39 De cellulaire en moleculaire mechanismen die vasten in werking stellen en die gezondheid verbeteren, lijken gunstig bij RA.40 (Zie ook artikel in VG 1-2020). Het aantal onderzoeken dat periodiek vasten direct linkt met klinische uitkomstmaten zoals RA is nog beperkt beschikbaar.41 Bovendien zijn de effecten van vasten bij RA van voorbijgaande aard en volhouden lijkt lastig.
Voedingssupplementen
Voedingssupplementen zijn naast een gezond voedingspatroon hulpmiddelen die bij uitstek geschikt zijn om ontsteking terug te dringen en weefsel te herstellen.
Probiotica
 Onderzoek naar de inzet van probiotica als ontstekingsremmer is nu volop aan de gang, echter met gemengde uitkomsten van klinische studies. Een meta-analyse, uitgevoerd door onderzoekers van de universiteit van Shiraz (Iran), vond geen significante daling van de ontstekingsmarkers TNFα, IL1β, IL6, IL10 en IL12, of van markers voor oxidatieve stress. Wel was er een verbetering in ziekteactiviteit dankzij probiotica. Deze meta-analyse telde vier studies met een totaal aan 153 patiënten. Hun conclusie staat in contrast met een eerder verschenen meta-analyse uitgevoerd door Egyptische, Syrische, Japanse en Vietnamese onderzoekers. Ze vonden geen vermindering van ziekteactiviteit, maar wel een daling van IL6, dit op basis van negen studies met 361 patiënten.45,46 Recent verscheen een review en meta-analyse betreffende het effect van probiotica op inflammatoire biomarkers bij volwassenen. In totaal werden 42 gerandomiseerde klinische studies (1138 deelnemers in de interventiegroep and 1120 deelnemers in de controlegroep) geïncludeerd. De onderzoekers concludeerden dat suppletie met probiotica de serumconcentraties van pro-inflammatoire cytokines zoals hsCRP, TNFα, IL6, IL12 en IL4 significant verlaagde. Probiotica hadden geen invloed op IL1B-, IL8-, IFNγ- en IL17- concentraties. Tenslotte stelden de onderzoekers een significante toename van IL10-concentraties vast.47 De klinische effecten van probiotica en reuma zijn vooralsnog onduidelijk.46 Onderzoek naar associaties tussen darmmicrobiota en ziekteactiviteit zal in de toekomst helpen om te begrijpen hoe ook voeding via het darmmicrobioom RA kan beïnvloeden.
Onderzoek naar de inzet van probiotica als ontstekingsremmer is nu volop aan de gang, echter met gemengde uitkomsten van klinische studies. Een meta-analyse, uitgevoerd door onderzoekers van de universiteit van Shiraz (Iran), vond geen significante daling van de ontstekingsmarkers TNFα, IL1β, IL6, IL10 en IL12, of van markers voor oxidatieve stress. Wel was er een verbetering in ziekteactiviteit dankzij probiotica. Deze meta-analyse telde vier studies met een totaal aan 153 patiënten. Hun conclusie staat in contrast met een eerder verschenen meta-analyse uitgevoerd door Egyptische, Syrische, Japanse en Vietnamese onderzoekers. Ze vonden geen vermindering van ziekteactiviteit, maar wel een daling van IL6, dit op basis van negen studies met 361 patiënten.45,46 Recent verscheen een review en meta-analyse betreffende het effect van probiotica op inflammatoire biomarkers bij volwassenen. In totaal werden 42 gerandomiseerde klinische studies (1138 deelnemers in de interventiegroep and 1120 deelnemers in de controlegroep) geïncludeerd. De onderzoekers concludeerden dat suppletie met probiotica de serumconcentraties van pro-inflammatoire cytokines zoals hsCRP, TNFα, IL6, IL12 en IL4 significant verlaagde. Probiotica hadden geen invloed op IL1B-, IL8-, IFNγ- en IL17- concentraties. Tenslotte stelden de onderzoekers een significante toename van IL10-concentraties vast.47 De klinische effecten van probiotica en reuma zijn vooralsnog onduidelijk.46 Onderzoek naar associaties tussen darmmicrobiota en ziekteactiviteit zal in de toekomst helpen om te begrijpen hoe ook voeding via het darmmicrobioom RA kan beïnvloeden.
Omega-3-vetzuren
De westerse voeding is over het algemeen laag in omega-3-vetzuren en hoog in omega-6-vetzuren. Meervoudig onverzadigde vetzuren (MOV’s ) spelen een centrale rol bij de homeostase van het immuunsysteem. Een overmaat aan omega-6-vetzuren werkt overwegend pro-inflammatoir, terwijl omega-3-vetzuren anti-inflammatoire eigenschappen hebben. Data uit diermodellen hebben geleid tot de hypothese dat suppletie met omega-3-vetzuren veelbelovend is in de preventie en behandeling van RA. Bij mensen zijn het tot nu toe slechts casestudies en prospectieve cohortstudies die een verband aantonen tussen een hoog gehalte aan omega-3-vetzuren in de voeding en een lagere kans op het ontwikkelen van RA bij deelnemers met een verhoogd risico. Sommige studies bevestigen de rol van omega-3-vetzuren als een waardevolle behandeloptie voor patiënten met RA, in het bijzonder voor het verminderen van pijn, aantal gevoelige gewrichten, duur van de ochtendstijfheid en de behoefte aan NSAID’s.48
In een prospectieve studie met 205 vrouwen met RA werd een associatie gevonden tussen inname van omega-3-vetzuren (> 2100 mg per dag) en een 35%-verlaging van het risico op het ontwikkelen van RA vergeleken met een lagere inname. Het langdurig gebruiken van meer dan 2100 mg per dag was geassocieerd met een 52% lager risico.49
Er is enig bewijs dat het nemen van borageolie in combinatie met reguliere analgetica of NSAID’s de symptomen van RA kan helpen verminderen na zes weken behandeling. De verbetering houdt aan tot 24 weken na de behandeling. Borageolie kan de ‘tender joint score’ met 45% verlagen en de ‘swollen joint score’ met 41%.50
Vitamine D
Vitamine D speelt een belangrijke rol in het immuunsysteem en om die reden ook in de pathofysiologie van RA. RA-patiënten zijn vaak vitamine D-deficiënt.51 In de COMORA-studie werd duidelijk dat lage vitamine D-spiegels geassocieerd zijn met verhoogde ziekteactiviteit, corticosteroïdedosis en comorbiditeit.52 Vitamine D heeft anti-inflammatoire effecten, mogelijk door de onderdrukking van IL17+- en IFNγ+-T-cellen. T-cellen in de synoviale vloeistof lijken minder gevoelig voor vitamine D. Een andere rol die vitamine D zou kunnen spelen is het verlagen van de kans op osteoporose en het verminderen van angst en depressie bij RA-patiënten.53
Antioxidanten
 Er is sprake van een toename in het oxidatieve-stressniveau bij RA.54 Echter de onderbouwing voor toepassingen van antioxidantsuppletie is tegenstrijdig.55 In een Iraanse studie kregen 39 vrouwen met mild tot matig ernstige RA gedurende 12 weken dagelijks een capsule met 50 mcg selenium, 8 mg zink, 400 mcg vitamine A, 125 mg vitamine C en 40 mg vitamine E. De onderzoekers stelden een significante reductie vast in serum-hsCRP en DAS28-score.56 Ook is er een significante associatie tussen lage serumseleniumspiegels en RA.57 Lage serumconcentraties van albumine, zink en selenium zijn onafhankelijk gerelateerd aan de ziekteactiviteit-index in een evaluatie van spoorelementen in 110 patiënten met RA.58
Er is sprake van een toename in het oxidatieve-stressniveau bij RA.54 Echter de onderbouwing voor toepassingen van antioxidantsuppletie is tegenstrijdig.55 In een Iraanse studie kregen 39 vrouwen met mild tot matig ernstige RA gedurende 12 weken dagelijks een capsule met 50 mcg selenium, 8 mg zink, 400 mcg vitamine A, 125 mg vitamine C en 40 mg vitamine E. De onderzoekers stelden een significante reductie vast in serum-hsCRP en DAS28-score.56 Ook is er een significante associatie tussen lage serumseleniumspiegels en RA.57 Lage serumconcentraties van albumine, zink en selenium zijn onafhankelijk gerelateerd aan de ziekteactiviteit-index in een evaluatie van spoorelementen in 110 patiënten met RA.58
Vitamine E in combinatie met de standaardbehandeling is effectiever dan de standaardtherapie voor het verminderen van pijn, maar niet voor het verminderen van inflammatie bij patiënten met RA.59
Co-enzym Q10 verlaagde de DAS28-score van 5,01 naar 2,34 bij reumapatiënten die twee maanden lang een supplement namen. Ook daalde het serumniveau matrixmetalloproteïnase-3 (MMP3) in de co-enzym Q10-groep, terwijl die in de controlegroep toenam. Iraanse onderzoekers bevestigden deze bevinding in een gecontroleerde studie met 54 reumapatiënten die 100 mg co-enzym Q10 per dag namen, of een placebo. Op basis van de DAS-score werd een daling van het aantal gezwollen en gevoelige gewrichtsplekken naar nul in de coQ10-groep waargenomen. De pijnscore ging ook sterk omlaag, van 63 naar 7 punten.60
MSM, glucosamine en chondroïtine
MSM wordt vaak gecombineerd met andere bestanddelen zoals glucosamine en chondroïtine. In-vitro-studies laten een anti-inflammatoir effect van MSM zien middels reductie van de cytokine-expressie.67 Vergelijkbare resultaten zijn gevonden in diermodellen.68,69 MSM in combinatie met glucosamine en chondroïtinesulfaat verminderde C-reactief proteïne (CRP) in ratten met geïnduceerde acute en chronische RA.70
De meeste humane studies maken voor het vastleggen van resultaten slechts gebruik van subjectieve vragenlijsten. Deze klinische studies laten zien dat MSM effectief is in het verminderen van pijn.71-73 Ook werden verbeteringen vastgesteld in stijfheid en zwelling. In de studie van Usha versterkte MSM in combinatie met glucosamine de verbeteringen in pijn, pijnintensiteit en zwelling.71 Pijn en stijfheid door RA verbeterde ook met een combinatie van glucosamine, chondroïtinesulfaat en MSM.74,75 Ten slotte bleek MSM ook pijn te verminderen als het werd gebruikt in combinatie met type II-collageen.77
Kruiden
Onderbouwing voor kruiden is overwegend empirisch, aangevuld met dierstudies, in-vitro- en in-vivo-studies en gericht op werkingsmechanismen en actieve bestanddelen van plantenextracten. Een samenvatting is terug te vinden in een uitgebreide review van Dragos.61
In de beschikbare klinische studies is niet gekeken naar het effect van plantenextracten op ziekteprogressie. Hiervoor zijn studies met een langere looptijd nodig. Het nadeel van behandeling met plantenextracten is de interactie met reguliere medicatie, soms lage biologische beschikbaarheid, afwezigheid van standaardisatie, gebrek aan nationale en internationale richtlijnen en daarmee de mogelijkheid tot vervalsing.62-65 Ik beperk me tot een overzicht van de kruiden en hun actieve fytonutriënten in tabel 1. Referenties zijn terug te vinden in de review die gratis te downloaden is.61
| Arnica montana | valkruid of wolverlei | fenolzuren en flavonoïden |
| Boswellia serrata | boswellia | frankinsence, boswelliazuren, |
| curcuma spp. | kurkuma | curcumine, béta-elemeen |
| Equisetum arvense | heermoes | kynureenzuur |
| Harpagofytum procumbens | duivelsklauw | iridoïde-glycosiden (bitterstoffen) o.a. harpagoside |
| salix spp. | wilg | salicine, polyfenolen en flavonoïden |
| Panax notoginseng | ginseng | saponinen |
| Sesamum indicum | sesam | lignanen, sesamine en sesamoline |
| Symphytum officinale | smeerwortel | fenolzuren (rozemarijnzuur), glycopeptides en aminozuren |
| Zingiber officinalis | gember | polyfenolen: gingerolen en shogaolen |
| Withania somnifera | ashwagandha | withaferine A |
tabel 1 Kruiden en hun actieve fytonutriënten die in staat zijn pro-inflammatoire cytokines te verlagen en potentie hebben klinische symptomen van RA te verbeteren.61
Conclusie
Hoewel RA-patiënten vaak te horen krijgen dat voeding slechts in beperkte mate bijdraagt aan het ontstaan en de progressie van RA, hebben sommige groepen patiënten wel degelijk baat bij specifieke voedingsinterventies. Echter de beschikbare literatuur rechtvaardigt geen officiële voedingsrichtlijnen voor RA als (gedeeltelijke) vervanging van reguliere medicatie.
Er is beperkte onderbouwing voor plantaardige voeding, mediterrane voeding en voor eliminatie van onder andere gluten. Helaas is het vaak lastig deze voedingsaanpassingen vol te houden. Dysbiose is een belangrijk aspect van RA en voeding kan het darmmicrobioom beïnvloeden en wellicht hierdoor ook de ziekteactiviteit. Deze rol lijkt ook weggelegd voor probiotica, echter de onderbouwing is nog beperkt. Voedingssupplementen zoals vitamine D, omega-3-vetzuren en antioxidanten kunnen op maat geadviseerd worden. Kortom er zijn voldoende aanwijzingen dat er een rol is weggelegd voor voeding, suppletie en leefstijl.7 Echter onderzoek met voeding is complex en kost veel tijd. Gelukkig is er momenteel volop aandacht voor de rol van voeding en leefstijl bij ziekte.