Het is een universeel gegeven dat baby's wenen als ze
neergelegd worden. Als we de moeite nemen om te luisteren, zullen
onze neuronen en hormonen de juiste respons aanmoedigen. Baby's
zijn geconcipieerd om frequent gevoed te worden op een manier die
huid-op-huidcontact, vasthouden en beschikbaarheid van
gelaatssignalen vereist. Hieruit resulteren heilzame en
permanente veranderingen, zowel bij ouder als kind. Voldaan
(gelukkig) moederlijk gedrag groeit als de signalen gevolgd
worden.
Ook voor versterking van vaderlijk gedrag is gezorgd. Participatie van de vader moedigt zijn verdere betrokkenheid aan en zorgt voor overeenstemming tussen vader en moeder. Veelvuldige nabijheid en huidcontact tussen baby en ouders kan sterke familiebanden creëren, met vele voordelige langetermijneffecten.
Spijtig genoeg werden in de loop van de laatste eeuw ouders door industrieel geschoolde 'experten' aangemoedigd tot ontkenning van díe instincten, die moeten zorgen voor natuurlijke 'ouderschapslessen'. Psychologen, neurologen en biochemici hebben nu bevestigd wat velen al instinctief vermoedden: dat vele 'beloningen' van het ouderschap daardoor gemist werden. Maar ook dat hele generaties kinderen hierdoor verstoken werden van belangrijke, levenslange voordelen.
Het nemen van beslissingen als volwassene
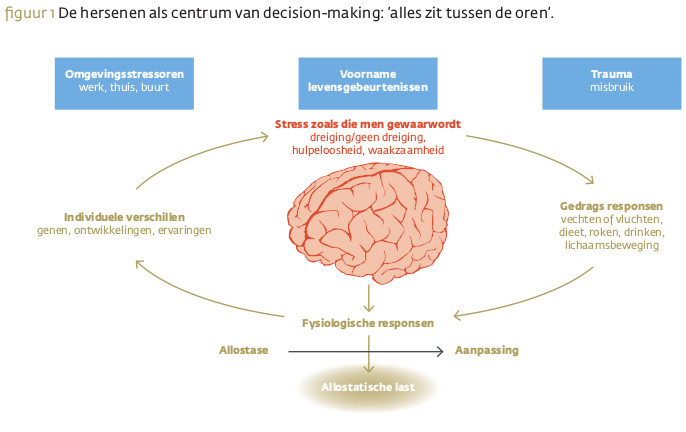
Zoals dit artikel probeert aan te tonen is het nemen van beslissingen moeilijk, dit wordt beïnvloed door meerdere biochemische pathways en gereguleerd door verschillende regio's van het centraal zenuwstelsel. Decision-making (DM) is relatief makkelijk in periodes van weinig stress. Stressvolle omstandigheden versterken echter de neiging om beslissingen te nemen gebaseerd op emotionele waarden, en zijn daarom zeer 'beloningsgevoelig'. Directe beloningsgevoeligheid kan leiden tot binge eating, een 'lui fenotype’ en een hoger risico op vallen en onverwacht overlijden (Liu-Ambrose 2012, Pruimboom 2011, Peters 211, Schultz 2006).
Stresstolerantie bepaalt DM in stressvolle periodes, en deze hangt af van meerdere parameters, zoals fysische conditie, socio-economische status, beroep, voedingstoestand, vroege ervaringen en zelfs transgenerationele factoren. Mensen met een hoge stresstolerantie kunnen beschouwd worden als resilient (veerkrachtig, flexibel), ze zullen leren van hun beslissingen, zelfs als deze niet de beste was. Niet-veerkrachtige mensen hebben een lagere flexibiliteit en leercapaciteit, wat leidt tot cirkelgedrag met herhaling van de verkeerde beslissingsstrategieën, alhoewel ze ‘weten’ dat deze verkeerd zijn (Ortin 2012).
McEwen toonde recent aan hoe chronische psychosociale stress interageert met omgevingstoxines (gifstoffen), en hoe deze interactie verantwoordelijk is voor lage executieve functies (EF) en een hogere mortaliteitsincidentie dan verwacht.
Flexibele, tolerante personen zullen beslissingen nemen die voordelig zijn, zowel voor zichzelf, als voor familieleden en vrienden. Niet-veerkrachtige mensen hebben echter de neiging te kiezen voor opties met een 'directe beloning' om de activiteit van de centrale assen te inhiberen (McEwen 2011, Starcke 2010, Esch 2010).
Decision-making is geen lineair proces. Het belangrijkste verschil tussen het menselijk brein en zelfs de zwaarst mogelijke computer is dat menselijke DM onvoorspelbaar is (alhoewel niet noodzakelijk), in tegenstelling tot beslissingen van de computer, om het simpele feit dat ieder programma opgemaakt is door mensen (Sheppes 2011).
Het is interessant te zien dat het menselijk oordeel in oorzakelijke redeneringsproblemen normaal wel beter is dan statistische methodes of computeralgoritmen (Trueblood 2012). Mensen zien namelijk gemakkelijker (verborgen) oorzakelijke verbanden, ook als er niet genoeg informatie is voor statistieken (Kushnir 2003), maar hun causale redenering is niet onfeilbaar. Subjectief oordelen kan vaak afwijken van de regels van de 'probabiliteitstheorie'. Bekende voorbeelden zijn te vinden in de rechtspraak, waar door menselijke interferentie een eindbeslissing vaak afhangt van de wijze en volgorde waarin de bewijzen worden gepresenteerd (Hogarth 1992).
Omdat zeer veel factoren DM beïnvloeden, en DM essentieel is voor de menselijke gezondheid, lijkt het cruciaal dat individuen leren hun vrije wil te gebruiken, zelfs in stressvolle situaties (Pruimboom 2008). Als mensen 'pre-sstressed' zijn (d.w.z. hoog cortisol), zullen emotionele dilemma's 'egoïstisch' gedrag tot gevolg hebben (Starcke 2010).
Samenvattend kan men stellen dat het effect van stress op beslissingen relevant kan zijn voor de volksgezondheid. De nadelige effecten van stress op de gezondheid zijn goed gedocumenteerd. Stress zou het risico verhogen op cardiovasculaire, psychiatrische en psychosomatische ziekten, en het stimuleert tevens ongezond gedrag zoals roken, drinken en ongezonde voeding (Juster 2010, McEwen 2008, Schneiderman 2005).
Stress kan dus zowel directe als indirecte effecten hebben op gezondheid, en deze effecten worden gemedieerd door de suboptimale beslissingen van het individu, die onmiddellijke beloning verschaffen, ten koste van negatieve langetermijngevolgen (Starcke 2012).
Hoe de achtergrond begrijpen en een interventie opmaken
EF en cognitieve flexibiliteit (CF) zijn de twee basale parameters in relatie tot optimale besluitnamevaardigheid. Ze worden beïnvloed door emotionele uitdagingen, nutritionele en socio-economische status, beroep, slaap, niveau aan beweging, ervaringen in het vroege leven, cultuur, omgevingstoxines, en transgenerationele factoren. Al deze factoren beïnvloeden DM door veranderingen in de energie-toewijzing aan de hersenregio's die essentieel gerelateerd zijn aan DM.
Energie-allocatie naar de hersenen is een gevolg van hersenbloedstroom, die zuurstof en nutriëntentransport naar de hersenen faciliteert. De hersenbloedstroom is een dynamisch proces dat gereguleerd wordt door het activiteitenpatroon van de twee centrale stressassen: het sympathische zenuwstelsel en de HPA-as (Bosma 2012, Peters 2011, Zlokovic 2011, Eskes 2010). Peters et al. toonden aan dat de hersenen, of het brein, selfish (egoïstisch) is (zie The selfish brain) op gebied van energie en grondstoffenallocatie, zelfs als andere organen zouden kunnen lijden onder de (pathologische) gevolgen van deze fundamentele biologische drijfveer (Pruimboom 2012).
De zogenaamde pull-push-regeling tussen het brein (pull, de hersenen 'trekken' energie binnen) en de omgeving (push) is ontstaan om de hersenen te voorzien van voldoende energie, dit ten koste van obesitas, ziekte, en indien nodig, de inductie van een non-permissive brain disorder' (Pruimboom 2011).
Een optimaal functionerend individu gebruikt voor energie een 'brein-pull-mechanisme' in stressvolle situaties: dit faciliteert DM, EF en CF. Een intacte stressasrespons verhoogt de hersenbloedstroom en de energie-allocatie naar de hersenen door hersenregio's te activeren in hiërarchische volgorde (Peters 2011). Stressvolle situaties induceren koolhydraatcraving (niet afhankelijk van zoetheid), wat ontstaan van glucopenie en slecht humeur lijkt te voorkomen na een stress-challenge (Hitze 2010).
Een gezond individu onder chronische psycho-emotionele stress behoudt dit 'brein-pull-systeem' met een hogere activiteit van het sympathische zenuwstelsel (SAM) en HPA-reactiviteit, wat uiteindelijk leidt tot gewichtsverlies en eetlustverlies (Peters 2011).
Maar wat gebeurt er als de stresassen hun responsiviteit verliezen door gewenning aan chronische activatie? Flaa toonde aan dat iemand met een lagere SAM-respons na een acute stresstest de neiging heeft om meer bij te komen dan diegenen met een hogere SAM-respons (Flaa 2008).
De lagere SAM-respons na acute stress zou kunnen verklaard worden door het hogere rustniveau van (nor)adrenaline bij mensen die gevoelig zijn voor stressgeïnduceerde gewichtstoename. Dit hogere rustniveau lijkt het gevolg van het verlies van negatieve feedback op niveau van de centrale SAM-regulatie, dat oorzaak is van een constante productie van noradrenaline en adrenaline, in plaats van de normale ritmische activiteit. De hogere sympaticus-tonus in rust leidt tot catecholamine-resistentie in vetweefsel en spieren, en dit tot lagere lipolytische activiteit en gebrek aan gluconeogenese (Bosma 2012, Faulds 2003, Hellstrom 1997). Om de basale metabole snelheid te behouden van de hersenen, die hun fysiologische pull-systeem verloren hebben, moet de voedselinname verhoogd worden (Peters 2011). Overeten zal dan leiden tot energieopslag in vetweefsel en spieren, oorzaak van obesitas en inflammatie.
[[{"fid":"4772","view_mode":"default","fields":{"format":"default","field_file_image_alt_text[und][0][value]":"","field_file_image_title_text[und][0][value]":""},"type":"media","attributes":{"height":"1646","width":"2548","class":"media-element file-default"}}]]
Cerebrovasculaire reserve
DM, EF en CF tijdens stresssituaties hangen echter af van de hersenbloedstroom (CBF), en deze is verstoord bij mensen die lijden aan alzheimer, dementie en depressie (Zlokovic 2011). De CBF-respons tijdens stresssituaties is de belangrijkste motor om genoeg energie en grondstoffen te voorzien voor de cruciale hersenregio's die instaan voor oplossingsgericht gedrag (Peterson 2011). De upregulering van CBF wordt de 'cerebrovasculaire reserve' genoemd.
Cerebrovasculaire reserve is dus de capaciteit van de hersenbloedvaten om te reageren op verhoogde metabole vraag en chemische, mechanische en neurale stimuli (Davenport 2012). CBF wordt gereguleerd door diverse mechanismen, wat het belang aantoont van het behoud van de hersenfuncties in (bijna) iedere situatie (Peterson 2011).
NO speelt een centrale rol in de cerebrovasculaire reserve. NO-productie is geïnhibeerd bij endotheeldisfunctie, bij hoge vrijeradicalenstress en bij lagere opname/hoger verbruik van arginine (Vita 2011). NO-inducerende interventie zouden dus als basaal moeten beschouwd worden voor het herstel van de energie-allocatie naar de hersenen, en verbetering van EF, CF en DM.
Het gebruik van het aminozuur L-arginine als supplement of via argininerijke voedingsmiddelen lijkt hier dus geïndiceerd (Cuevas 2004).
Actuele interventies
EF en CF kunnen verbeterd worden door diverse interventies, o.a. door acute of chronische beweging, specifieke voedingsmiddelen, psychotherapie, choline- en magnesiumsuppletie (Davenport 2013, Chang 2012, Slutsky 2010, Zeisel 2009). Choline, omega-3-vetzuren en magnesium lijken het meest beloftevol, indien gesuppleerd in voldoende hoge dosis (Slutsky 2010, Zeisel 2009).
Choline
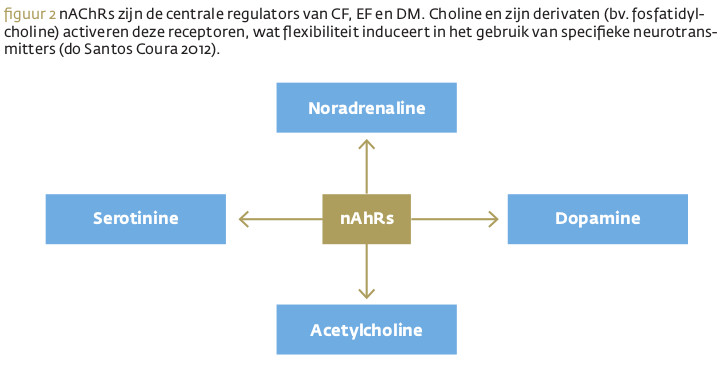
Bijzonder interessant is hierbij choline (als precursor van acetylcholine), omdat het de productie en gevoeligheid lijkt te reguleren van alle andere neurotransmitters die CF, EF en DM beïnvloeden (do Santos Coura 2012). In deze context zijn choline en zijn derivaten verantwoordelijk voor de meerderheid aan functies gerelateerd aan werkgeheugen, taak-shift en reversal learning (do Santos Coura). Choline wordt beschouwd als een semi-essentieel nutriënt met een hogere behoefte in situaties van verlengde stress (fysisch en psychisch), ziekte, verandering in de omgeving en stijgende leeftijd (Ziesel 2009). Het gebruik van cholinerijke voeding zou daarom moeten beschouwd worden als basaal in de behandeling van mensen die leiden aan lage EF en CF, evenals aan obesitas en overgewicht, auto-immuunziekten, dementie, alzheimer, CVS en FM, en andere pathologieën die de hersenhomeostase aantasten.
Lage cholinevoorziening induceert een cholinedistributie volgens het model van hiërarchische prioriteiten: choline uit nier, long en darm zal herverdeeld worden naar lever en hersenen, wat mogelijk schade zal veroorzaken aan deze organen, die disposable (‘verwaarloosbaar') zijn voor directe overleving en reproductie (McCann 2011, Li 2008, Kirkwood 2008). Langdurige cholinedeficiëntie kan leiden tot zware schade aan deze organen, en zelfs tot cerebrale cholinedeficiëntie, wat aan de basis kan liggen van alzheimer en andere neurodegeneratieve ziekten (Li 2008).
Choline komt voor in verscheidene voedingsmiddelen, belangrijke bronnen zijn eidooier, vis en schaaldieren, groene bladgroenten en vlees van wild. De minimale dagelijkse behoefte is 500 mg. De maximum inname is gesteld op 3,5 gram, hogere doses kunnen leiden tot een 'visachtige' lichaamsgeur, braken, verhoogde speekselvorming en zweten, en lage bloeddruk (FDA 1998).
De optimale behandeling: het BERN-concept
De optimale behandeling voor EF, CF en DM is het gebruik van een geïntegreerd programma gebaseerd op gedragsinterventies, beweging, relaxatie en voeding, met name het BERN-concept van stressmanagement:
Behaviour | > | Incl. aangename activiteiten, sociale interactie en ondersteuning, vriendschap, liefde, gezonde communicatie … |
Exercise | > | Aërobe en anaërobe fysische activiteit |
Relaxation | > | Inclusief meditatie, spiritualiteit/geloof, slaaphygiëne |
Nutrition | > | Voeding, inclusief suppletie indien nodig |
Daarnaast kunnen cognitieve gedragstherapie en andere therapeutische modellen, zoals mind-bodygeneeskunde toegevoegd worden.
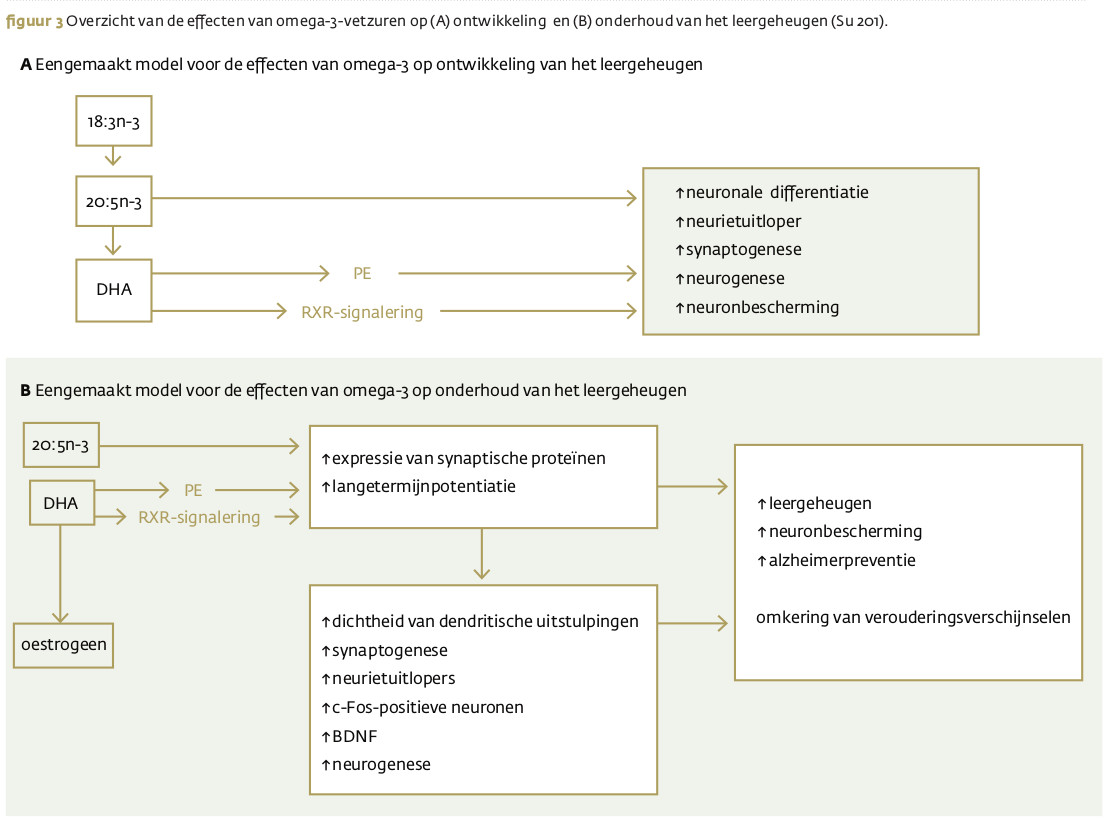
Omega-3-vetzuren
Er is reeds lang bewezen dat deze effectief zijn in de behandeling van patiënten met EF en CF-stoornissen (Yurko-Mauro 2010). De pathways hoe deze EF, CF en DM kunnen verbeteren, evenals de totale functionering van het centraal zenuwstelsel, werden recent opnieuw geëvalueerd (Su 2010).
Magnesium
Magnesium lijkt een van de veelbelovendste nutriënten te zijn in de behandeling van verlies van cognitieve functies in het algemeen, maar speciaal bij mensen die lijden aan neurodegeneratieve pathologieën (Abumaria 2011, Slutsky 2010). Magnesiumdeficiëntie kan beschouwd worden als de belangrijkste pro-inflammatoire factor volgens de inflammatie-index van Cavicchia (2009). Meer recent toonde Weglicki (2012) aan dat magnesiumdeficiëntie beschouwd moet worden als de belangrijkste aandrijving voor ontsteking van het centraal zenuwstelsel. Magnesiumrijke nutriënten zouden dus deel moeten uitmaken van de 'whole food'-behandeling bij mensen die lijden aan lage EF en CF. Magnesium functioneert als een natuurlijke calcium-antagonist, induceert de productie van NO, verhoogt de cerebrale reserve, en is sterk anti-inflammatoir. Magnesiumdeficiëntie is zeer veel voorkomend, de oorzaken voor tekort alomtegenwoordig.
Magnesiumrijke voeding: groene groenten (chlorofyl), noten, chocolade ...
Besluit
Decision making (DM) is de belangrijkste allostatische capaciteit van de Homo sapiens. En DM bepaalt onze keuzes: inzake het juiste voedsel en compliance (dieet en therapie), investeren in fysische activiteit, samenwerken met anderen, altruïstisch gedrag … Deze zijn allemaal afhankelijk van de beslissingen die we nemen. Factoren zoals voeding, cultuur, ervaringen vroeg in het leven, micronutriënten deficiënties, beweging, geslacht en leeftijd beïnvloeden DM door wijzigingen op het niveau van executieve functie (EF) en cognitieve flexibiliteit.
Chronische ziekte is vaak het gevolg van het nemen van de verkeerde beslissingen, en het lijden aan chronische ziekten verhoogt het risico op lage EF en CF.
Behandeling van alle patiënten zou daarom moeten beginnen met het meten van EF en CF, met het gebruik van gevalideerde instrumenten zoals de Iowa gambling test, de Wisconsin card sorting test en de cijfersymbool-substitutietest. Als de EF aangetast is dan zou BERN-gebaseerde therapie eerst de DM-capaciteit moeten verbeteren, om pas daarna ziektespecifieke therapie toe te passen. Therapietrouw hangt immers af van EF, en daarom kan enkel EF de naleving en werkzaamheid van de therapie verbeteren.